Étude de phase I du traitement de la leucémie myéloïde aiguë (LMA) à l’aide de cellules LMA autologues modifiées pour exprimer l’IL-12
Du 23 avril 2018 au 31 mars 2023
Renseignements clés

- Cette approche thérapeutiquea le potentiel d’améliorer defaçon marquée les soins auxpatients qui ont une LMA enrechute grâce à de meilleursrésultats et un risque detoxicité fortement réduitpar rapport aux traitementscourants
- Cette approche surmontebon nombre des défisassociés au traitementcourant qui repose surl’utilisation de moelle osseusede donneur
- La nature systémique de cettethérapie peut éradiquer uneleucémie qui s’est répandue
- Cette approche peut setraduire par une mémoireimmunologique à longterme qui est formée pourreconnaître et attaquer lescellules souches cancéreusesgrâce à l’utilisation despropres cellules cancéreusesd’un patient sous forme deplateforme vaccinale.
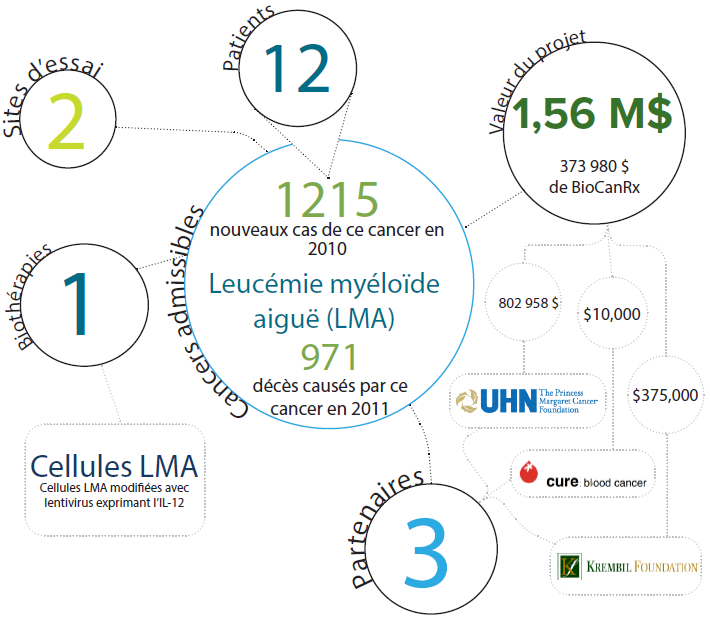
À propos du projet
Le système immunitaire a la capacité de tuer les cellules leucémiques si on lui indique correctement de le faire. Certaines des directives clés se présentent sous la forme de protéines solubles qui, si elles sont présentes dans les quantités appropriées, aident les cellules du système immunitaire à reconnaître les cellules leucémiques et à s’activer pour les tuer.
L’équipe du projet a déjà démontré que les cellules leucémiques peuvent être modifiées pour sécréter l’une de ces protéines, appelées interleukine 12, ou IL-12. Dans les systèmes expérimentaux, les cellules leucémiques qui sécrètent de l’IL-12 ont stimulé une réponse immunitaire robuste qui, une fois initiée, a continué à tuer toutes les cellules leucémiques résiduelles, même celles qui ne sécrètent pas d’IL-12. La leucémie myéloïde aiguë (LMA) est une maladie potentiellement mortelle pour laquelle, dans de nombreux cas, il n’existe pas de traitement curatif. Ce projet mettra à l’essai la sécurité de l’approche qui consiste à injecter à un groupe de 10 à 12 patients certaines de leurs propres cellules LMA qui ont été modifiées pour sécréter de l’IL-12.
L’essai clinique déterminera si une réponse immunitaire a été initiée dans le sang et la moelle osseuse du patient à mesure que le traitement se poursuit. Il surveillera également l’effet du traitement sur le niveau de la maladie et suivra chaque patient pendant deux ans.


